В ГКБ им. И.В. Давыдовского спасли пациентку с грыжей Морганьи
Женщина, 56 лет, приехала на лечение в Москву из Рязанской области с жалобами на дискомфорт в области желудка и на одышку при физической нагрузке, длившимися около 6 месяцев. Её мучила сильная изжога, сложности с глотанием пищи, жжение в желудке.
Женщина обратилась в Городскую клиническую больницу им. И.В. Давыдовского и была госпитализирована в больницу в плановом порядке.
После проведениях всех необходимых диагностических исследований, пациентке был поставлен редкий диагноз — грыжа пищеводного отверстия диафрагмы, грыжа Морганьи.
По КТ было определено, что у пациентки диафрагмальная грыжа больших размеров с проникновением клетчатки малого и большого сальника, петель тонкой кишки, поперечной и нисходящей ободочной кишки, желудка, 12-перстной кишки в грудную полость. Также при КТ выявлен дефект передних отделов диафрагмы — грыжа Морганьи.
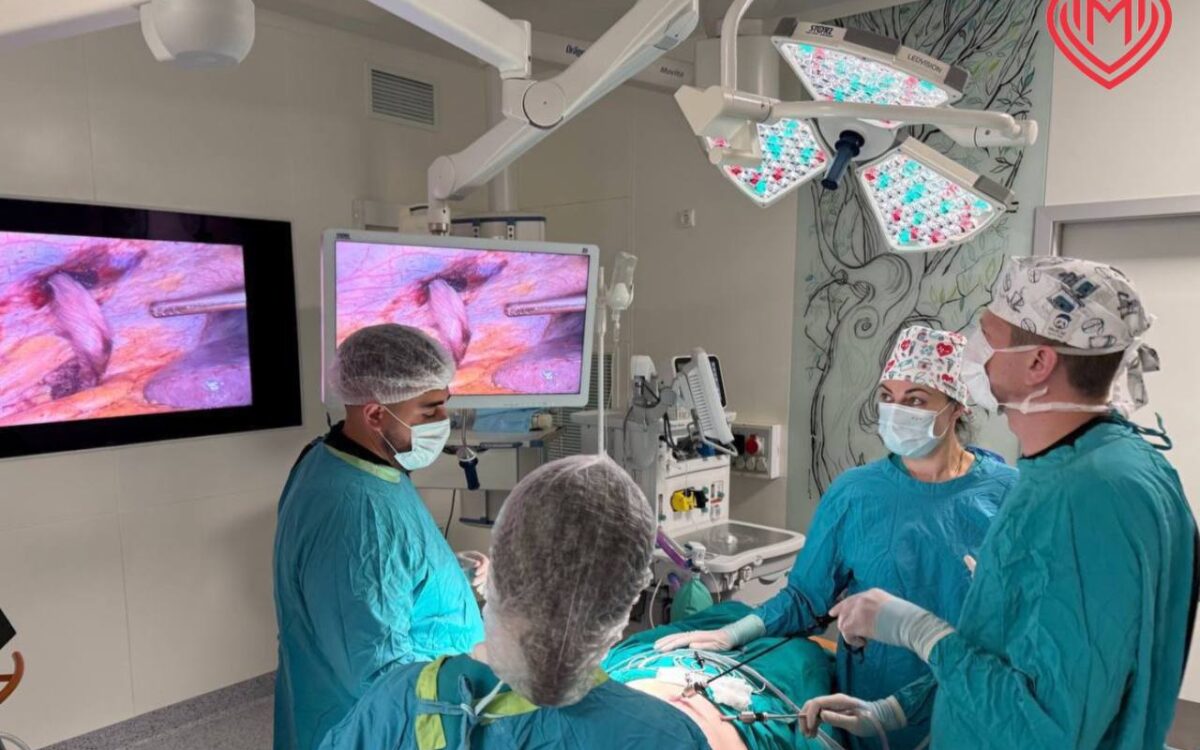
Бригада хирургов больницы произвели лапароскопическую фундопликацию по Ниссену в модификации Черноусова: передняя и задняя пластика пищеводного отверстия диафрагмы (крурорафия), удаление кисты левой доли печени, пластика грыжи Морганьи местными тканями, дренирование брюшной полости», — пояснили в ГКБ им. И.В. Давыдовского.
Жалобы пациентки были связаны с тем, что большое количество внутренних органов петель тонкой и толстой кишки, желудка, обоих сальников и другое — были перемещены выше диафрагмы, смещая легкие и органы средостения.
«Если говорить коротко, то за три часа операции пищевод и желудок низведены в брюшную полость, сформирована фундопликационная манжета, выполнена передняя и задняя пластика пищеводного отверстия диафрагмы (крурорафия). Из диафрагмальной грыжи Морганьи выделена и удалена липома, сам грыжевой дефект ушит. Выявленная киста левой доли печени была резецирована.
Технической особенностью данной операции было проведение симультанного лапароскопического оперативного пособия при двух, самостоятельно сложных и редко встречающихся патологиях, каждая из которых у данной пациентки имела свои анатомические особенности.
После выписки все симптомы, вызывающие дискомфорт и плохое качество жизни пациентки, прошли», — рассказал А.Б. Шалыгин, заместитель директора по хирургической помощи ГКБ им И.В. Давыдовского.
Восстановление и выписка пациента были проведены в короткие сроки — через 5 дней женщина поехала домой.
«Оснащение московских больниц и квалификация наших врачей сегодня находится на высочайшем уровне, не уступая, а иногда и превосходя многие мировые клиники. Это позволяет нам проводить операции экспертного уровня, после которых реабилитационный период у пациентов проходит в очень короткие сроки, а также дает возможность пациентам жить полноценной жизнью, забывая о своих недугах», —
добавил Э.А. Галлямов, д.м.н., профессор, зав. кафедрой общей хирургии Первого МГМУ им. И.М. Сеченова.










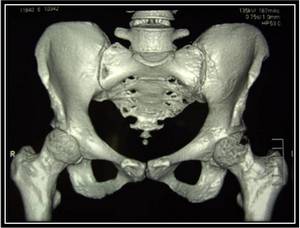
 Остеомиелит таза (ОТ) представляет собой собирательное понятие, которое включает в себя целую группу заболеваний, характеризующихся костно-деструктивными изменениями бактериальной этиологии, но существенно отличающихся по патогенезу. При этом ряд особенностей заставляет выделить остеомиелит таза в отдельную группу. Это массив тазовых костей, трудная доступность очагов инфекции, расположенные рядом внутренние органы, магистральные сосуды, нервные стволы. Все это определяет трудности как диагностики, так и лечения остеомиелита таза. Данный вид костной патологии, как правило, протекает тяжелее остеомиелита другой локализации. Характерные для ряда форм остеомиелита таза запоздалая диагностика и несвоевременно начатое лечение определяют высокую частоту развития сепсиса, а также многолетнее рецидивирующее течение заболевания. Еще одной особенностью остеомиелита таза является частое мультифокальное поражение, создающее дополнительные трудности в диагностике. Традиционно выполняемая при обследовании больных обзорная рентгенография при ОТ
Остеомиелит таза (ОТ) представляет собой собирательное понятие, которое включает в себя целую группу заболеваний, характеризующихся костно-деструктивными изменениями бактериальной этиологии, но существенно отличающихся по патогенезу. При этом ряд особенностей заставляет выделить остеомиелит таза в отдельную группу. Это массив тазовых костей, трудная доступность очагов инфекции, расположенные рядом внутренние органы, магистральные сосуды, нервные стволы. Все это определяет трудности как диагностики, так и лечения остеомиелита таза. Данный вид костной патологии, как правило, протекает тяжелее остеомиелита другой локализации. Характерные для ряда форм остеомиелита таза запоздалая диагностика и несвоевременно начатое лечение определяют высокую частоту развития сепсиса, а также многолетнее рецидивирующее течение заболевания. Еще одной особенностью остеомиелита таза является частое мультифокальное поражение, создающее дополнительные трудности в диагностике. Традиционно выполняемая при обследовании больных обзорная рентгенография при ОТ отличается малой информативностью, способствуя диагностическим ошибкам. Чаще всего наблюдается ОТ гематогенного происхождения. Значительно реже встречаются посттравматический, послеоперационный, огнестрельный и контактный остеомиелит. Среди тазовых костей остеомиелитом чаще поражаются крыло и тело подвздошной кости, а также крестцово-подвздошное сочленение.
отличается малой информативностью, способствуя диагностическим ошибкам. Чаще всего наблюдается ОТ гематогенного происхождения. Значительно реже встречаются посттравматический, послеоперационный, огнестрельный и контактный остеомиелит. Среди тазовых костей остеомиелитом чаще поражаются крыло и тело подвздошной кости, а также крестцово-подвздошное сочленение. Рис. 1. Схематическое изображения направления вне- и внутритазовых затеков при ОТ. Сагиттальный срез. Как видно из схемы, гной может распространяться как внутрь таза, так и наружу, под ягодичные мышцы и межмышечно, имитируя постинъекционную флегмону.
Рис. 1. Схематическое изображения направления вне- и внутритазовых затеков при ОТ. Сагиттальный срез. Как видно из схемы, гной может распространяться как внутрь таза, так и наружу, под ягодичные мышцы и межмышечно, имитируя постинъекционную флегмону. Рис. 2. Повышенное накопление РФП в области левого крестцово-подвздошного сочленения при ОТ.
Рис. 2. Повышенное накопление РФП в области левого крестцово-подвздошного сочленения при ОТ.
 Рис. 4. КТ таза. Мультипланарная реконструкция. Определяется костная деструкция в области крестцово-подвздошного сочленения.
Рис. 4. КТ таза. Мультипланарная реконструкция. Определяется костная деструкция в области крестцово-подвздошного сочленения. Рис. 5. КТ таза. 3D-реконструкция. Остеомиелитическая деструкция лобковой кости.
Рис. 5. КТ таза. 3D-реконструкция. Остеомиелитическая деструкция лобковой кости. Рис. 6. КТ пациентки с остеомиелитом подвздошной кости после эндопротезирования тазобедренного сустава.
Рис. 6. КТ пациентки с остеомиелитом подвздошной кости после эндопротезирования тазобедренного сустава. Рис. 7. Фистулограмма больного остеомиелитом таза. Определяются множественные свищи внутри- и внетазовой локализации.
Рис. 7. Фистулограмма больного остеомиелитом таза. Определяются множественные свищи внутри- и внетазовой локализации. Рис. 8. Фистулограмма. Массивный затек под ягодичные мышцы у пациентки с остеомиелитом седалищной кости.
Рис. 8. Фистулограмма. Массивный затек под ягодичные мышцы у пациентки с остеомиелитом седалищной кости. тяжелых форм остеомиелита таза: гнойного сакроилеита. Особенность данной локализации в том, что при поражении массивных в этой зоне костей (подвздошной и крестца) формируются параоссальные гнойные полости и свищи как вне-, так и внутритазовой локализации. Наиболее рациональным в этом случае будет комбинированный доступ: внетазовый с отсечением ягодичных мышц, дополняемый внутритазовым внебрюшинным доступом к сочленению с кожным разрезом по краю гребня подвздошной кости. Данный доступ позволяет выполнить адекватную хирургическую обработку очага и эффективно дренировать его с помощью проточно-аспирационной системы. Резекция крестцово-подвздошного сочленения может сопровождаться формированием сквозного дефекта.
тяжелых форм остеомиелита таза: гнойного сакроилеита. Особенность данной локализации в том, что при поражении массивных в этой зоне костей (подвздошной и крестца) формируются параоссальные гнойные полости и свищи как вне-, так и внутритазовой локализации. Наиболее рациональным в этом случае будет комбинированный доступ: внетазовый с отсечением ягодичных мышц, дополняемый внутритазовым внебрюшинным доступом к сочленению с кожным разрезом по краю гребня подвздошной кости. Данный доступ позволяет выполнить адекватную хирургическую обработку очага и эффективно дренировать его с помощью проточно-аспирационной системы. Резекция крестцово-подвздошного сочленения может сопровождаться формированием сквозного дефекта.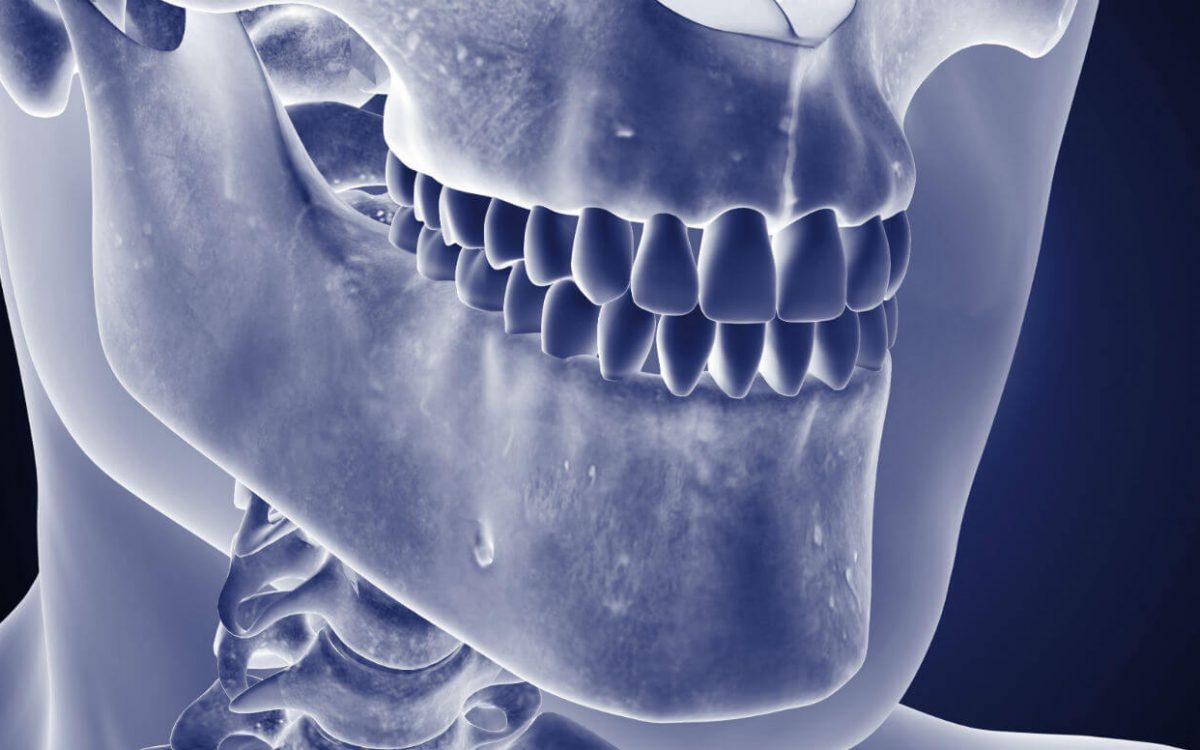
 Рис.1. Контактный остеомиелит лучевой кости у пациента оперированного по поводу запущенной флегмоны предплечья. В ране определяется лишенный надкостницы нежизнеспособный участок (серого цвета) диафиза лучевой кости.
Рис.1. Контактный остеомиелит лучевой кости у пациента оперированного по поводу запущенной флегмоны предплечья. В ране определяется лишенный надкостницы нежизнеспособный участок (серого цвета) диафиза лучевой кости. Рис. 2. Контактный остеомиелит лицевого скелета у пациентки, перенесшей тяжелую анаэробную инфекцию лица одонтогенного происхождения (старое название — нома).
Рис. 2. Контактный остеомиелит лицевого скелета у пациентки, перенесшей тяжелую анаэробную инфекцию лица одонтогенного происхождения (старое название — нома).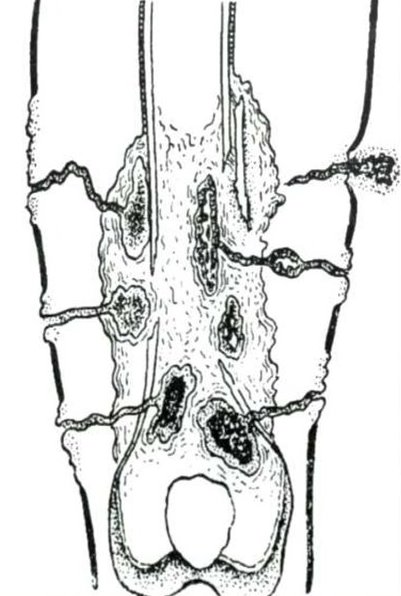


 Рис. 3. Дефект большеберцовой кости 12 см после ее сегментарной резекции по поводу посттравматического остеомиелита, несросшегося перелома. С целью стабилизации фрагментов и проведения дистракционно-компрессионного остеосинтеза наложен аппарат Илизарова. Для формирования дистракционного регенерата в проксимальном отделе кости выполнена поперечная остеотомия.
Рис. 3. Дефект большеберцовой кости 12 см после ее сегментарной резекции по поводу посттравматического остеомиелита, несросшегося перелома. С целью стабилизации фрагментов и проведения дистракционно-компрессионного остеосинтеза наложен аппарат Илизарова. Для формирования дистракционного регенерата в проксимальном отделе кости выполнена поперечная остеотомия. Рис. 4. В течение 4-х месяцев за счет постепенной дистракции сформирован костный регенерат необходимой длины. Дефект кости замещен. В подобном положении необходимо дождаться «созревания» дистракционного регенерата, который в настоящий момент еще не имеет достаточной минерализации, и консолидации «стыкованных» костных фрагментов в области диафиза.
Рис. 4. В течение 4-х месяцев за счет постепенной дистракции сформирован костный регенерат необходимой длины. Дефект кости замещен. В подобном положении необходимо дождаться «созревания» дистракционного регенерата, который в настоящий момент еще не имеет достаточной минерализации, и консолидации «стыкованных» костных фрагментов в области диафиза. Рис. 5. Рентгенограмма через 4 месяца. Дистракционный регенерат приобрел костную плотность. Отмечается образование костной мозоли между стыкованными фрагментами. Аппарат может быть демонтирован. Восстановлена длина и опороспособность конечности.
Рис. 5. Рентгенограмма через 4 месяца. Дистракционный регенерат приобрел костную плотность. Отмечается образование костной мозоли между стыкованными фрагментами. Аппарат может быть демонтирован. Восстановлена длина и опороспособность конечности.
Свежие комментарии