ПОСЛЕОПЕРАЦИОННЫЙ ОСТЕОМИЕЛИТ
Послеоперационный остеомиелит представляет собой воспалительный процесс в костной ткани, который развивается как гнойное осложнение в различные сроки после «чистых» операций на костях.
Наиболее частыми примерами таких операций будут: металлоостеосинтез (выполненный по поводу перелома) и эндопротезирование сустава (например, в связи с остеоартрозом). Механизм возникновения заболевания очень похож на тот, который мы наблюдаем при посттравматическом остеомиелите: травма кости с локальным нарушением ее кровоснабжения (в результате операции, предшествующей травмы).
Тем не менее выделение послеоперационного остеомиелита в отдельную группу вполне оправдано по двум причинам:
1) это послеоперационное осложнение, которое необходимо учитывать,
2) остеомиелит, который развивается в области металлоконструкции (костного фиксатора, эндопротеза сустава) имеет существенные особенности в лечении.
На особенностях лечения этого заболевания стоит остановиться подробнее. Возникновение остеомиелита в зоне имплантата по классическим канонам хирургии требует удаления последнего, который является инородным телом, способным поддерживать воспалительный процесс. Но возникает вопрос, к чему приведет его удаление? К сожалению, с этого момента основные проблемы могут нарастать как снежный ком.
Разберем наиболее типичные ситуации:
1) Остеомиелит после накостного металлоостеосинтеза. В случае, если к моменту возникновения остеомиелита отмечена консолидация костных отломков, то металлофиксатор удаляют, и лечение остеомиелита проводят по стандартным методикам.
2) Сложнее ситуация, когда имеет место остеомиелит, но еще нет сращения отломков. В этом случае если металлоостеосинтез стабилен (конструкция продолжает надежно фиксировать костные отломки) и есть перспектива консолидации (данная оценка проводится на основании анализа комплекса факторов и требует серьезной профессиональной подготовки врача) имеет смысл сразу не удалять фиксатор, продолжая паллиативное лечение остеомиелита до сращения перелома. В этот период могут наблюдаться гнойные свищи или раны, являющиеся проявлением остеомиелита. После консолидации отломков хирургическое лечение проводится по схеме, описанной в 1) ситуации. Если металлоостеосинтез нестабилен/имеется резко выраженный гнойный процесс/нет перспектив по сращению перелома, то фиксатор удаляется, выполняется хирургическая обработка остеомиелитического очага (одномоментно или отсроченно). С целью дальнейшего лечения перелома обычно переходят к наружному внеочаговому остеосинтезу с помощью различных аппаратов внешней фиксации.
Развитие остеомиелита после эндопротезирования сустава может рассматриваться не просто как тяжелое гнойное послеоперационное осложнение, а как полная драматизма жизненная ситуация, где переплетаются медицинские, социальные и парамедицинские аспекты. Остеомиелит после имплантации искусственного сустава относится к числу поздних послеоперационных осложнений и развивается, как правило, спустя несколько месяцев или даже лет после операции. Лечение остеомиелита в этом случае предполагает удаление инфицированного эндопротеза наряду с хирургической санацией остеомиелитического очага. Что пациент получает в итоге даже если остеомиелит излечен? Отсутствующий сустав, нефункционирующая конечность, все признаки инвалидизации. Возможны ли варианты? Да, безусловно. Самый благоприятный из них — это повторное эндопротезирование (так называемое ревизионное) в сроки от 6 месяцев до 1 года после излечения остеомиелита. Естественно, что риск послеоперационных гнойных осложнений после ревизионного эндопротезирования значительно выше, чем после первичного, и ни о каких гарантиях, естественно, речь не может идти. К сожалению, в повторном эндопротезировании пациентам часто отказывают в связи с преклонным возрастом, сопутствующей патологией и др. Как быть в этом случае? Рекомендация одна: приспосабливаться к жизни в изменившихся условиях с существенными функциональными нарушениями и ограничениями. В этой связи весьма важен индивидуальный подход к лечению пациентов с остеомиелитом после эндопротезирования крупных суставов. С нашей точки зрения, весьма дальновидно будет взвесить все «за» и «против». Всегда ли так уж необходимо удалять инфицированный эндопротез? Оказывается, что не всегда. Если эндопротез выполняет свою функцию, стабилен, воспалительный процесс в окружающий тканях не сильно выражен (например, имеется гнойный свищ с небольшим количеством отделяемого), а перспективы повторного эндопротезирования туманны, можно предпринять попытку сохранения имплантата, проводя консервативное лечение и поддерживая функционирующий свищ. Во всех остальных случаях: выраженный гнойно-воспалительный процесс, нарушение функции, нестабильность эндопротеза — его удаление представляется неизбежным. Хотя, необходимо признать, что некоторые пациенты весьма неплохо приспосабливаются к жизни с отсутствующим суставом: формируется либо анкилоз, либо неоартроз.
 Рис. 1. Остеомиелит и параоссальная флегмона после накостного металлоостеосинтеза большеберцовой кости пластиной.
Рис. 1. Остеомиелит и параоссальная флегмона после накостного металлоостеосинтеза большеберцовой кости пластиной.
 Рис. 2. Остеомиелит после погружного остеосинтеза большеберцовой кости пластиной. 4 месяца после операции. Консолидации перелома нет, как нет и перспектив для этого. Необходимо удаление пластины, сегментарная резекция большеберцовой кости, наружный дистракционно-компрессионный остеосинтез по Илизарову.
Рис. 2. Остеомиелит после погружного остеосинтеза большеберцовой кости пластиной. 4 месяца после операции. Консолидации перелома нет, как нет и перспектив для этого. Необходимо удаление пластины, сегментарная резекция большеберцовой кости, наружный дистракционно-компрессионный остеосинтез по Илизарову.
 Рис.3. Остеомиелит после погружного металлоостеосинтеза ключицы пластиной. 5 месяцев после перелома. Имеет место консолидация костных отломков. Показано удаление фиксатора, остеонекрсеквестрэктомия
Рис.3. Остеомиелит после погружного металлоостеосинтеза ключицы пластиной. 5 месяцев после перелома. Имеет место консолидация костных отломков. Показано удаление фиксатора, остеонекрсеквестрэктомия

Рис. 4. Остеомиелит после эндопротезирования коленного сустава. Имеется функционирующий гнойный свищ со скудным отделяемым. Функция имплантата сохранена. Перифокальное воспаление не выражено. При этом имеет место тяжелая сопутствующая общетерапевтическая патология. От удаления эндопротеза решено воздержаться, проводя консервативное лечение.
 Рис. 5. Остеомиелит бедренной кости после эндопротезирования тазобедренного сустава. В связи с выраженным воспалительным процессом необходимо удаление имплантата, резекция бедренной кости с последующим решением вопроса о возможности ревизионного эндопротезирования.
Рис. 5. Остеомиелит бедренной кости после эндопротезирования тазобедренного сустава. В связи с выраженным воспалительным процессом необходимо удаление имплантата, резекция бедренной кости с последующим решением вопроса о возможности ревизионного эндопротезирования.

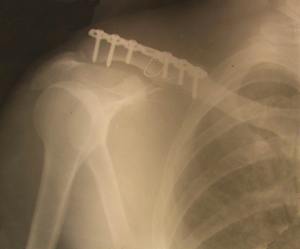
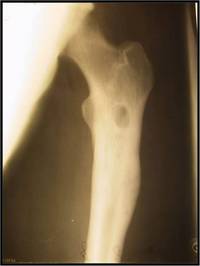


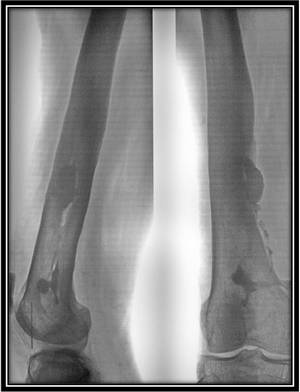
 Рис. 1. Наружное отверстие гнойного свища у больного хроническим гематогенным остеомиелитом бедренной кости. Определяются многочисленные рубцы после выполненных ранее хирургических вмешательств.
Рис. 1. Наружное отверстие гнойного свища у больного хроническим гематогенным остеомиелитом бедренной кости. Определяются многочисленные рубцы после выполненных ранее хирургических вмешательств. Рис. 2. Фистулограмма того же больного. Определяется утолщение и деформация пораженной остеомиелитом бедренной кости. Контрастное вещество, введенное в наружное отверстие свища, попадает в параоссальную и внутрикостную гнойные полости.
Рис. 2. Фистулограмма того же больного. Определяется утолщение и деформация пораженной остеомиелитом бедренной кости. Контрастное вещество, введенное в наружное отверстие свища, попадает в параоссальную и внутрикостную гнойные полости. Рис. 3. КТ того же больного. Определяется обширная остеомиелитическая полость в бедренной кости.
Рис. 3. КТ того же больного. Определяется обширная остеомиелитическая полость в бедренной кости. Рис. 4. ХГО локтевой кости. Последняя значительно утолщена и деформирована. В костной полости определяется секвестр.
Рис. 4. ХГО локтевой кости. Последняя значительно утолщена и деформирована. В костной полости определяется секвестр. Рис. 5. КТ бедренной кости. Поперечный срез на уровне дистального метаэпифиза. В остеомиелитической полости определяется свободно лежащий костный секвестр.
Рис. 5. КТ бедренной кости. Поперечный срез на уровне дистального метаэпифиза. В остеомиелитической полости определяется свободно лежащий костный секвестр. Рис. 6. Фистулограмма пациента, страдающего ХГО бедренной кости. Контрастируются множественные гнойные свищи, расположенные как в мягких тканях, так и проникающие в остеомиелитическую полость.
Рис. 6. Фистулограмма пациента, страдающего ХГО бедренной кости. Контрастируются множественные гнойные свищи, расположенные как в мягких тканях, так и проникающие в остеомиелитическую полость. Рис. 7. Рентгенологическая картина ХГО бедренной кости. Анамнез заболевания более 40 лет. Определяются выраженные структурные изменения бедренной кости (утолщение, деформация, множественные остеомиелитические полости с расположенными в них секвестрами). Для уточнения объема и характера деструктивных изменений необходимо выполнение КТ.
Рис. 7. Рентгенологическая картина ХГО бедренной кости. Анамнез заболевания более 40 лет. Определяются выраженные структурные изменения бедренной кости (утолщение, деформация, множественные остеомиелитические полости с расположенными в них секвестрами). Для уточнения объема и характера деструктивных изменений необходимо выполнение КТ.
 Рис. 9. Фистулограмма того же больного. Введенное в свищ контрастное вещество попадает внутрь кости, образуя депо в остеомиелитической полости в зоне проксимального метаэпифиза плечевой кости.
Рис. 9. Фистулограмма того же больного. Введенное в свищ контрастное вещество попадает внутрь кости, образуя депо в остеомиелитической полости в зоне проксимального метаэпифиза плечевой кости. Рис. 10. Рентгенограмма того же пациента после проведенного хирургического лечения. Выполнена трепанация плечевой кости с остеонекрсеквестрэктомией.
Рис. 10. Рентгенограмма того же пациента после проведенного хирургического лечения. Выполнена трепанация плечевой кости с остеонекрсеквестрэктомией.
 Рис. 2. Магнитно-резонансная томограмма пациента, страдающего острым гематогенным остеомиелитом таза (гнойный сакроилеит). Визуализируется выраженный воспалительный отек параоссальных мягких тканей.
Рис. 2. Магнитно-резонансная томограмма пациента, страдающего острым гематогенным остеомиелитом таза (гнойный сакроилеит). Визуализируется выраженный воспалительный отек параоссальных мягких тканей.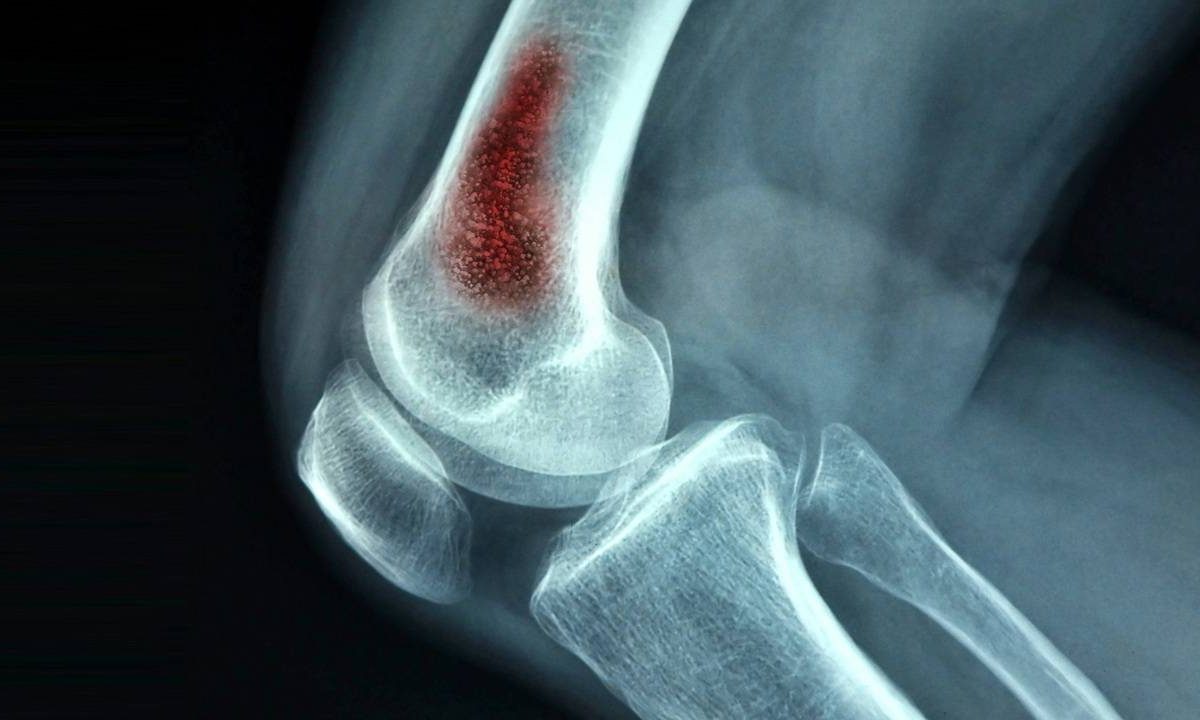
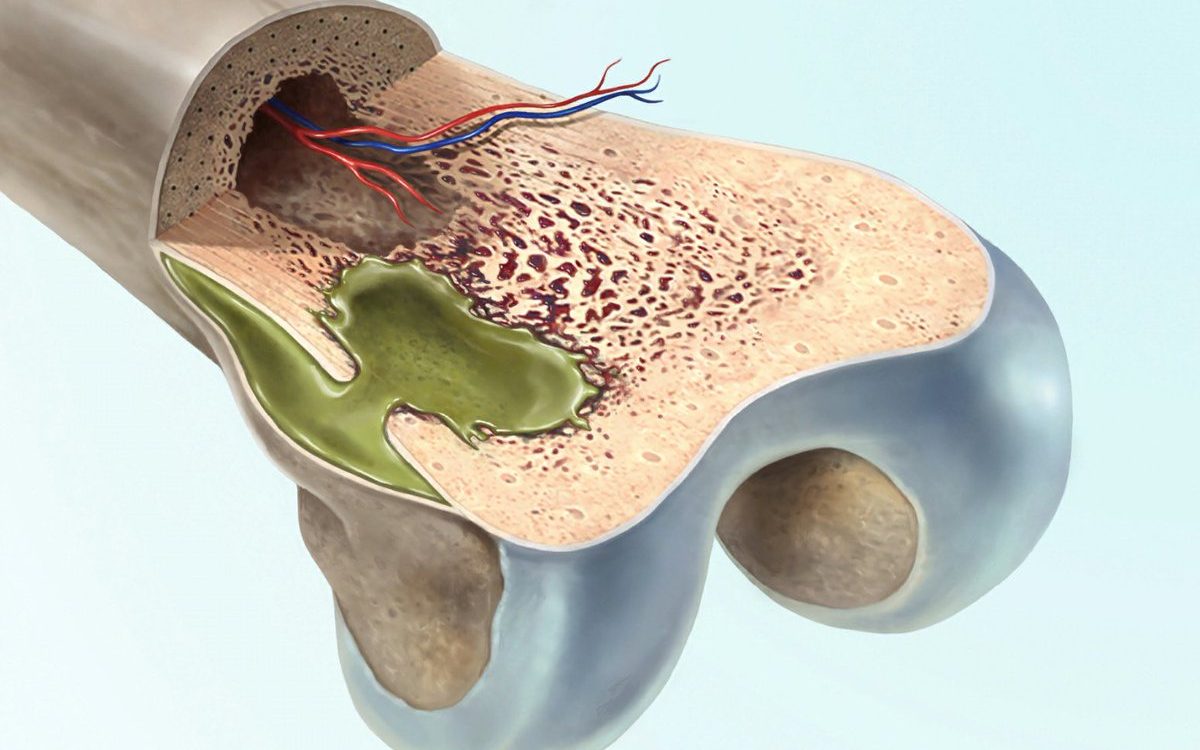







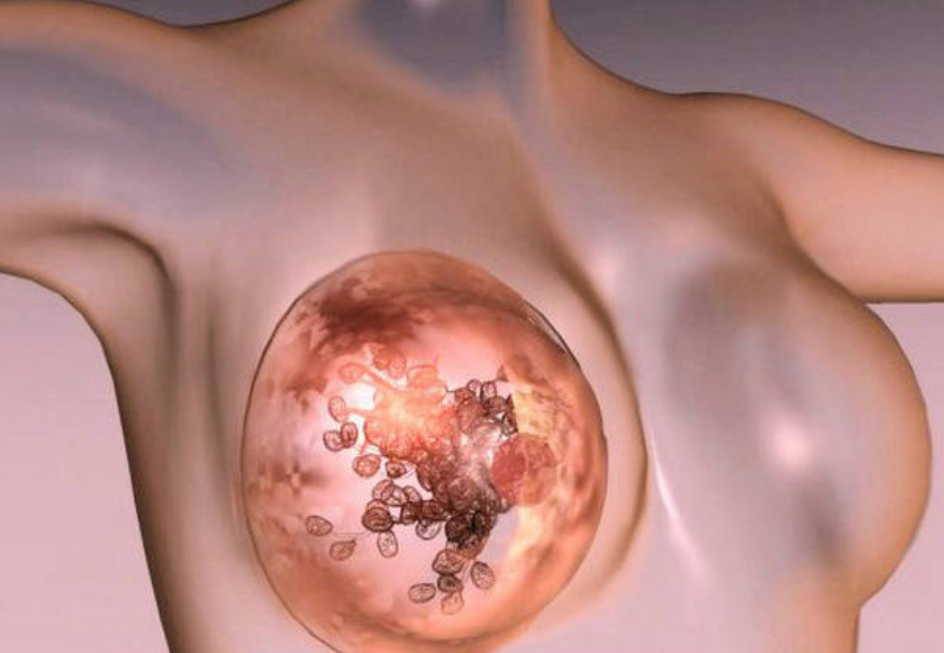
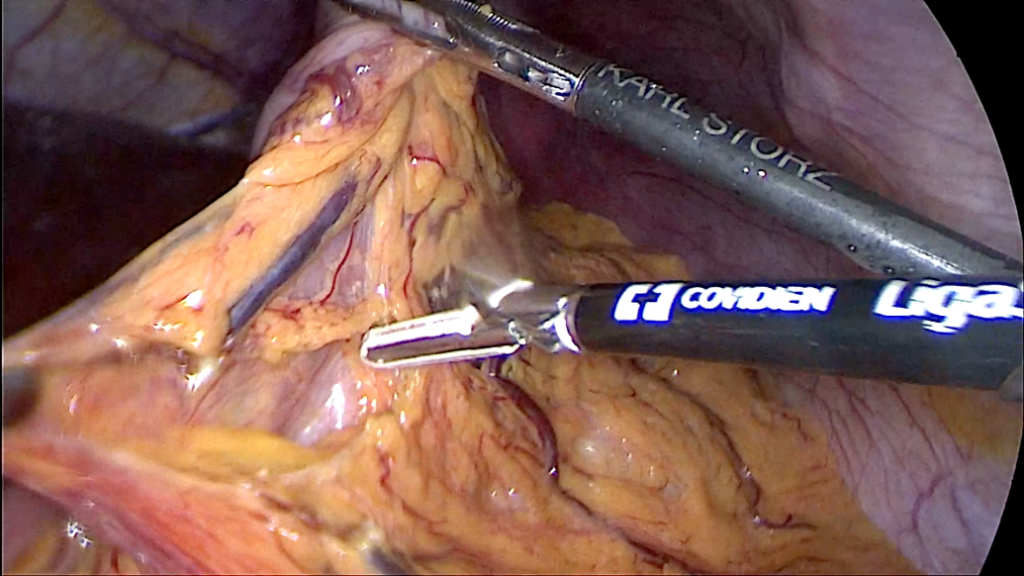
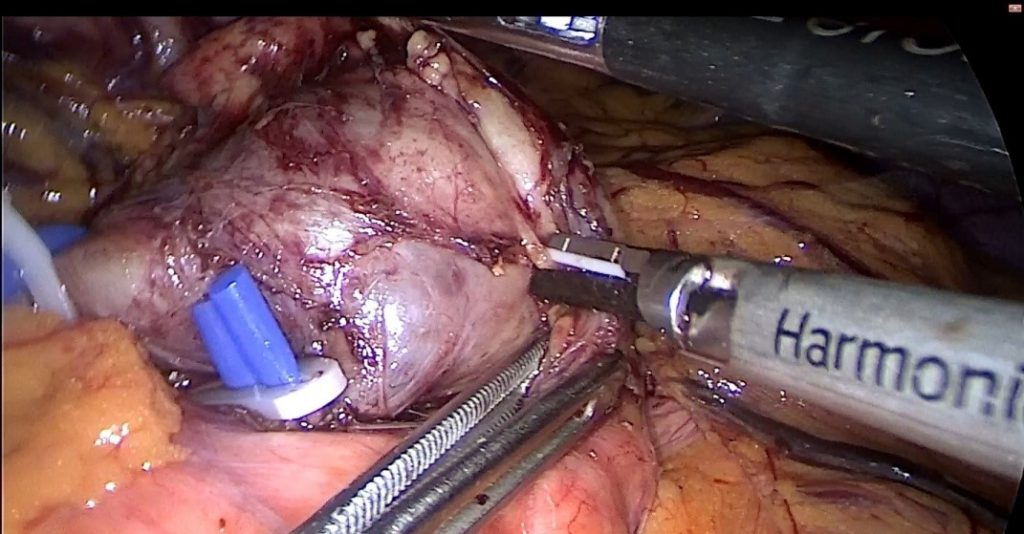
 Метод эндопротезирования молочных желез используется с 1958 г. С тех пор технология производства имплантатов постоянно совершенствуется, а результаты вмешательства чаще всего оцениваются как положительные. При этом различные осложнения, встречающиеся даже при использовании современных
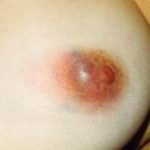
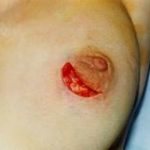
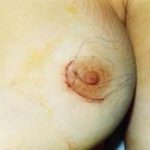
Метод эндопротезирования молочных желез используется с 1958 г. С тех пор технология производства имплантатов постоянно совершенствуется, а результаты вмешательства чаще всего оцениваются как положительные. При этом различные осложнения, встречающиеся даже при использовании современных  имплантатов, не являются редкостью и по данным различных авторов составляют от 6% до 30%. Правда, гнойные осложнения после эндопротезирования молочных желез составляют не более 1-4% среди всех осложнений, отличаясь при этом наибольшей тяжестью. Особенностью хирургического лечения данных пациенток является необходимость удаления инфицированных эндопротезов. В результате формируется деформация молочной железы и сопутствующий ей серьезный косметический дефект. Повторное эндопротезирование теоретически возможно и выполняется в сроки не ранее 6 месяцев после удаления инфицированного имплантата и ликвидации воспалительного процесса. При этот вероятность инфекционных осложнений несравнимо выше, чем после первичного эндопротезирования. Поэтому далеко не все пластические хирурги берутся оперировать подобных пациенток.
имплантатов, не являются редкостью и по данным различных авторов составляют от 6% до 30%. Правда, гнойные осложнения после эндопротезирования молочных желез составляют не более 1-4% среди всех осложнений, отличаясь при этом наибольшей тяжестью. Особенностью хирургического лечения данных пациенток является необходимость удаления инфицированных эндопротезов. В результате формируется деформация молочной железы и сопутствующий ей серьезный косметический дефект. Повторное эндопротезирование теоретически возможно и выполняется в сроки не ранее 6 месяцев после удаления инфицированного имплантата и ликвидации воспалительного процесса. При этот вероятность инфекционных осложнений несравнимо выше, чем после первичного эндопротезирования. Поэтому далеко не все пластические хирурги берутся оперировать подобных пациенток.


Свежие комментарии